Muchas veces decimos expresiones de este tipo: “vamos a tomar este vino en copas de cristal de Bohemia”, “ten cuidado que se ha roto una botella de vino y hay cristales en el suelo”, “tengo sucios los cristales de las ventanas”,“los cristales del coche están empañados”…. Técnicamente hablando estas expresiones no son correctas. Una cosa son cristales y otras son vidrios. Veamos la diferencia.
La materia está formada por átomos (y/o iones) que en determinadas ocasiones se juntan y forman lo que conocemos con el nombre de moléculas. Estos átomos o moléculas pueden encontrarse en tres estados gaseoso, líquido o sólido.
¿Qué es un cristal?
Un cristal es un estado sólido con una estructura organizada en las tres dimensiones. Los átomos, iones o moléculas que constituyen la estructura cristalina se encuentran dispuestos de forma regular que van reproduciendo un determinado esquema. Podemos decir que los átomos en un cristal arquitectónicamente ocupan unas posiciones precisas, un cristal es parecido a una molécula muy grande. Los cristales al disponer de un orden interno y repetitivo suelen mostrar una morfología externa regular con caras y aristas perfectamente definidas. Es decir un estado cristalino tiene una estructura perfecta.
Así por ejemplo, el cuarzo o cristal de roca que es un óxido de silicio, SiO2, los átomos de silicio y de oxígeno ocupan unas posiciones muy definidas. Cada átomo de silicio se une a cuatro átomos de oxígeno formando un tetraedro y esta estructura se va repitiendo. Véase figura 1.
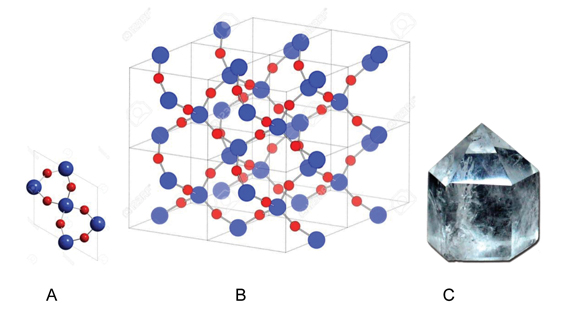
Otro ejemplo es el diamante, un cristal de carbono puro, en el que cada átomo de carbono se une a otros cuatro átomos de carbono y ocupa el centro de un tetraedro, y esta estructura se va repitiendo. La sal común o cloruro sódico, NaCl, es también un sólido cristalino.
¿Qué es un vidrio?
Cuando tenemos un material en que los átomos están colocados de una forma no ordenada, podríamos decir, caótica, con algunos enlaces que continúan conservándose pero ya no forman estructuras perfectas decimos que tenemos un vidrio. Los vidrios que son materiales amorfos en los que los átomos ya no mantienen un orden, en realidad, son líquidos sobreenfriados. Un líquido sobreenfriado es aquel que permanece como líquido a temperaturas más bajas que la de solidificación.
Podemos definir un vidrio como un producto inorgánico amorfo, constituido principalmente por sílice en un estado fundido/líquido que se ha enfriado hasta alcanzar una forma rígida con una viscosidad altísima y sin experimentar el proceso de cristalización. Así, por ejemplo los vidrios de silicato que utilizamos para las botellas, vasos, ventanas, parabrisas de los coches, espejos son fabricados con dióxido de silicio y otros compuestos como el carbonato cálcico, carbonato sódico, óxidos de plomo y carecen de estructura cristalina repetitiva.
Como podemos ver, figura 2, en un vidrio no hay regularidad perfecta, la disposición los átomos de silicio y los oxígenos se dispersan, podemos decir que se ha perdido la regularidad, por lo tanto esto no es un cristal, es un vidrio o sólido en estado vítreo.
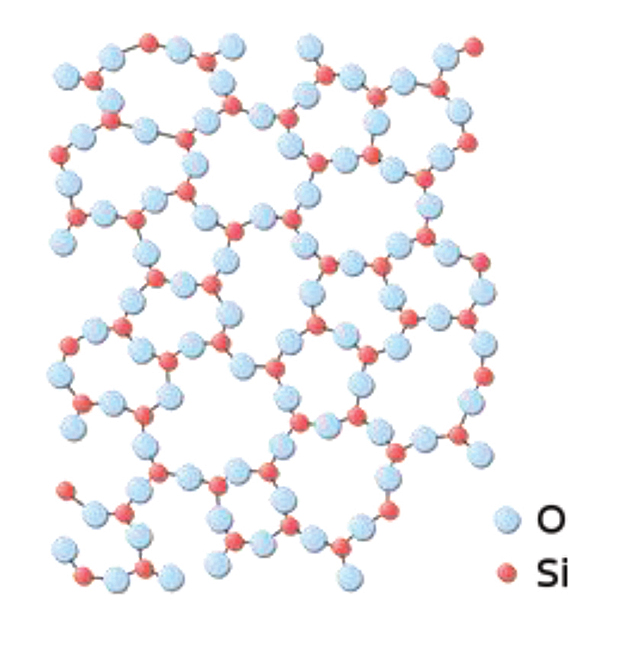
La sílice o dióxido de silicio, SiO2, como hemos visto puede cristalizar formando los cristales de cuarzo. Si calentamos la sílice hasta fundirla y enfriamos rápidamente, la sílice solidificará en estado amorfo y obtendremos la sílice vítrea, que es lo que denominamos vidrio común. La sílice funde a 1.713 ºC (temperatura de fusión) pero entre esa temperatura y 1.200 ºC (temperatura de transición vítrea) se produce lo que denominamos transición vítrea.
Como la temperatura de transición vítrea de la sílice es muy alta, para conseguir bajarla y mejorar algunas características, se utiliza sílice mezclada con otras sustancias, dando lugar a los diversos tipos de vidrios de silicatos.
El vidrio no se encuentra habitualmente en la naturaleza, salvo alguna excepción como es el caso de la “obsidiana”, una roca volcánica formada por silicatos alumínicos y óxidos silícicos fundidos que son expulsados en las erupciones volcánicas con un enfriamiento rápido en el exterior.
Cuando nos dicen que una copa de vino es de cristal, ¿han utilizado un cristal para hacer la copa de cristal?
Solo se encuentran cristales cuando ha habido un proceso que denominamos de cristalización. Este es el proceso en que los átomos, los iones o las moléculas se disponen de tal forma que minimice su estado energético formando, como que hemos visto, una red cristalina rígida y repetitiva. La entidad más pequeña de la red cristalina es lo que denominamos “célula unitaria”, la cual va aceptando átomos o moléculas y va creciendo formando un cristal macroscópico. Mientras transcurre este proceso, los átomos y las moléculas se enlazan formando ángulos bien definidos que van formando el cristal con caras y aristas bien definidas.
Múltiples cristalizaciones se ha producido y se sigue produciendo en la naturaleza, pero también se puede conseguir en el laboratorio o de forma industrial. En los siguientes enlaces se muestra como podéis hacer un experimento casero y conseguir cristales “gigantes” de la sal común o de azúcar.
Cuando decimos que una copa de vino es de cristal, no es cierto, es de lo que comúnmente llamamos “vidrio plomo” o “vidrio óptico”. La diferencia reside que en la elaboración vidrio, aparte de la sílice, se le ha añadido óxidos de plomo. Existen también la variedad de vidrios con óxidos de titanio. Es decir, lo que llamamos copas de cristal realmente son copas de vidrio de una calidad superior “premium”. Podemos encontrar copas de vino que son más baratas porque son de silicatos que no contienen plomo, y las de vidrio plomo serán más o menos caras según su contenido en plomo.
Copas de “cristal”, vidrio plomo, para el vino frente a las de vidrio sin plomo
La copa cumple un papel fundamental en el análisis de un vino.
Las de vidrio plomo son las ideales para la cata del vino en la fase visual al ser más transparentes, más brillantes e incoloras que las de vidrio sin plomo.
Tienen un sonido más fino al darles pequeños golpecitos. Ideales para los brindis y en especial para vinos espumosos al facilitar la liberación de pequeñas burbujas.
Permiten elaborar las copas con paredes más delgadas, aunque son más delicadas que las de vidrio simple. En la fase visual de la cata, también permiten observar mejor las lágrimas causadas por el efecto Marangoni.
Son algo más pesadas, cuanto mayor sea su porcentaje de plomo.

Copa de cata AFNOR
La Asociación Francesa de Normalización, conocida como AFNOR, estandarizó la copa para catar un vino. El objetivo de esta estandarización es que en las catas los vinos se analicen de la misma forma. Este hecho ha dado lugar a que la copa se denomine “copa AFNOR” (figura 3). Aceptada por la “International Organizationfor Standardization”, bajo la norma ISO 3591–1977. Esta copa también es la que acepta desde el año 2009 la Organización Internacional de la Viña y el Vino (OIV). Quiero señalar que algunos expertos no las consideran apropiadas para las catas y prefieren utilizar distintos tipos de copas.
Las características y peculiaridades de la “copa AFNOR”, son las siguientes:
– Altura total de la copa: 155 mm (±5)
– Altura del cáliz: 100 mm (±2)
– Altura del tallo y la base: 55 mm (±3)
– Diámetro del borde: 46 mm (±2)
– Diámetro del horizonte del cáliz: 65 mm (±2)
– Diámetro de la base: 65 mm (±5)
– Capacidad total de la copa: 215 mm (±10)
– Volumen de degustación (al Ecuador de la copa): 50 ml
– Grosor del cristal: 0,8 mm (±0,1)
– Grosor del tallo: 9 mm (±1)
– Realizada en cristal transparente incoloro con un porcentaje de plomo entre el 9 y el 12 por ciento.
Se recomienda el realizar una limpieza profunda de la copa, sin restos de detergente, olores, sin marcas y huellas de los dedos. Guardar las copas en un lugar exento de polvo y olores. Utilizar una copa distinta para cada vino o si no es posible “envinar” la copa, que consiste en enjuagar la copa entre un vino y otro, con el mismo vino que se catará a continuación.
La Organización Mundial de la Salud, recomienda que las copas no tengan más de un 24% de plomo. Puede tener algún riesgo para la salud dejar alimentos o bebidas almacenados durante mucho tiempo en envases de vidrio con plomo, ya que éste se va liberando muy lentamente. Sin embargo, el tiempo que se tiene el vino en una copa no supone riesgo alguno.
Se ha comentado que en los decantadores de vino de vidrio plomo, al dejar el vino almacenado durante mucho tiempo, se puede llega a notar que el vino se vuelve cada vez más dulce, esto es consecuencia del acetato de plomo (denominado por los romanos azúcar de plomo) que es dulce, y se va disolviendo lentamente en el vino.
El Comité Mixto FAO/OMS estableció para el plomo una PTWI (Provisional Tolerable Weekly Intake, ingesta semanal tolerable) de 25 microgramos/Kg/semana. La acción quelante de los polifenoles presentes en el vino tinto, probablemente disminuyen la absorción del plomo procedente de la dieta, por lo que la presencia de este metal en las copas de vino, teniendo en cuenta la PTW y el tiempo de permanencia del vino en la copa, no resulta en absoluto peligrosa. El tratar este tema, sería como dicen los ingleses, “pan para otro sándwich”.
MIGUEL POCOVÍ | Doctor en Ciencias y catedrático de Bioquímica y Biología Molecular



















